DIAGNOSTIC ET SUIVI DE LA DMLA
Qu'est-ce qu'un diagnostic?
Le terme diagnostic est défini par le dictionnaire Merriam-Webster comme « l'art ou l'acte d'identifier une maladie par ses signes et ses symptômes ».
En ce qui concerne la dégénérescence maculaire liée à l'âge (DMLA), cela signifie qu'un professionnel de la santé, tel qu'un ophtalmologue ou un optométriste, utilise divers tests et examens pour déterminer si un patient peut être atteint de DMLA.2 Ces techniques portent sur la fonction visuelle ainsi que sur des techniques d'imagerie permettant de visualiser la rétine et la macula au fond de l'œil. Nous vous présentons ici les différentes techniques de diagnostic liées à la DMLA.
La seule façon de diagnostiquer la DMLA est de faire effectuer un examen complet de l'œil, y compris un examen de la macula, par un optométriste ou un ophtalmologiste.
Il convient de noter que nombre de ces techniques sont également utilisées pour suivre un patient au fil du temps après le diagnostic de DMLA. Votre professionnel de santé vous dira à quelle fréquence vous devez vous rendre aux visites de suivi, et il est important de suivre ses conseils.
Contrôlez votre propre vision.
Si vous avez reçu un diagnostic de DMLA ou si vous risquez de développer une maladie oculaire, il est important de veiller à surveiller toute modification de votre vision.
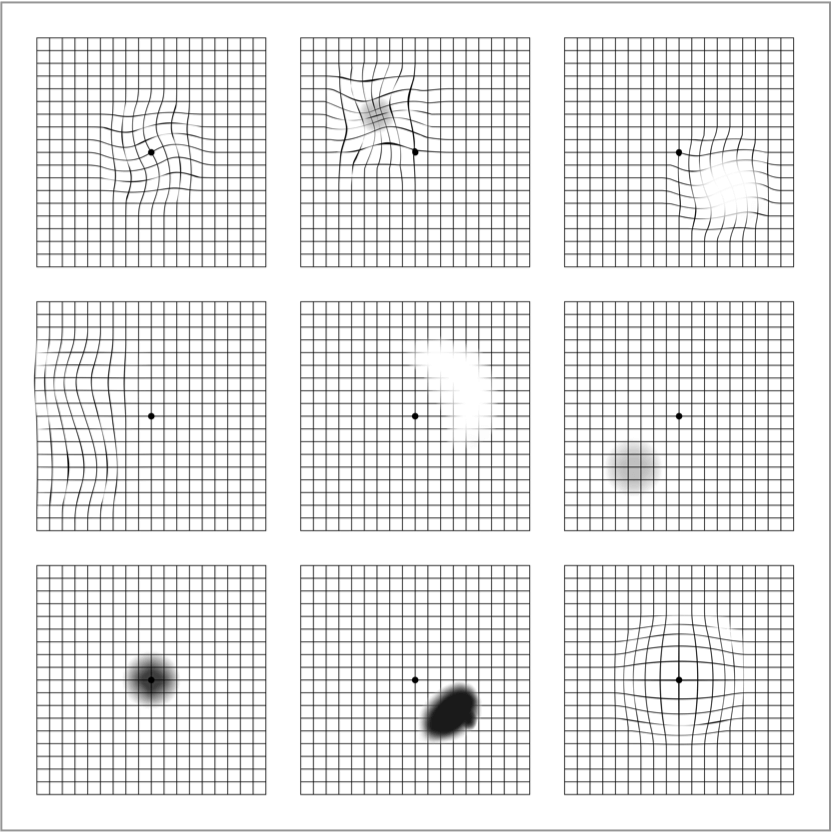
La grille d'Amsler est un outil d'autocontrôle essentiel1 et facile à utiliser pour détecter les changements précoces de votre vision. Ces changements peuvent inclure une distorsion (lignes droites apparaissant ondulées), des taches floues ou des taches sombres.
Il est important de ne pas se fier à la grille d'Amsler pour établir un diagnostic, et elle ne remplace pas un examen régulier des yeux. La seule façon de diagnostiquer la DMLA est de faire passer un examen de la vue, y compris un examen de la macula, par un optométriste ou un ophtalmologue. Notez que les modifications de la vision sur une grille d'Amsler peuvent également être le signe d'une autre maladie oculaire que la DMLA.

Si vous détectez des changements dans votre vision, il est important de consulter un optométriste ou un ophtalmologiste dès que possible.
Vous pouvez télécharger et imprimer une grille d'Amsler en cliquant sur le lien ci-dessous ou en vous rendant dans la section « outils de soutien » du site web. Le téléchargement comprend une grille d'Amsler ainsi que des instructions étape par étape sur la façon de l'utiliser pour contrôler votre propre vision.
La seule façon de diagnostiquer la DMLA est de faire effectuer un examen complet de l'œil, y compris un examen de la macula, par un optométriste ou un ophtalmologiste.
La section suivante donne un aperçu des examens qui peuvent être effectués.
Tests utilisés pour diagnostiquer et surveiller la dégénérescence maculaire liée à l'âge (DMLA)
Examens des yeux effectués par des optométristes ou des ophtalmologues.
La seule façon de diagnostiquer la DMLA est de faire faire un examen complet de l'œil, y compris un examen de la macula, par un optométriste ou un ophtalmologiste.2 La section suivante présente une vue d'ensemble des examens qui peuvent être effectués par un ophtalmologiste. Veuillez noter que tous les tests ne seront pas effectués par votre professionnel de santé et que les tests utilisés peuvent différer selon les pays. Si vous avez des questions concernant l'un de ces tests, vous devez les poser à votre professionnel de santé lors de votre prochaine visite.
En général, les tests les plus courants utilisés pour le diagnostic et le suivi de la DMLA sont les suivants :
• Examen complet des yeux
• Examen du fond d'œil
• Ophtalmoscopie
• Photographie du fond de l'œil
• Tomographie par cohérence optique (OCT)
• Angiographie à la fluorescéine du fond de l'œil
Les tests les moins courants utilisés pour le diagnostic et le suivi de la DMLA sont les suivants :
• Angiographie au vert d'indocyanine
• Microperimétrie
• Acuité visuelle à faible luminosité
• Le tableau d'acuité de MNRead
• Examen de la sensibilité aux contrastes
• L'indice fonctionnel d'autonomie en lecture
Veuillez vous référer à la section suivante pour une description plus détaillée des tests énumérés ci-dessus.
Tests utilisés pour diagnostiquer et surveiller la dégénérescence maculaire liée à l'âge (DMLA)
Examen complet de la vue
Le principal symptôme des personnes atteintes de DMLA est une perte de la vision. Par conséquent, la DMLA est souvent diagnostiquée lors d'un examen oculaire de routine. Un examen complet de l'acuité visuelle mesure la capacité d'une personne à voir les détails, les formes et les lettres à une certaine distance.3 La meilleure acuité visuelle corrigée (BCVA) est normalement évaluée à l'aide d'une carte de Snellen, mais notez que d'autres cartes peuvent également être utilisées par votre professionnel de santé. Le nombre de lettres qu'une personne peut identifier correctement représente son acuité visuelle. En d'autres termes, plus une personne peut lire vers le bas de l'échelle de Snellen, meilleure est son acuité visuelle.3

Examen du fond d'œil
L'examen du fond d'œil est un test plus approfondi pour aider à diagnostiquer la DMLA. Il s'agit d'un examen optique de la rétine, située au fond de l'œil. Notez que le fond de l'œil est un terme médical désignant la partie d'un organe la plus éloignée de l'ouverture, et dans ce cas, il s'agit de l'arrière de l'œil. L'examen du fond d'œil peut être réalisé par ophtalmoscopie ou par photographie du fond d'œil.2 Dans les deux cas, des gouttes dilatantes sont appliquées sur l'œil du patient pour permettre au praticien de mieux voir l'arrière de l'œil.4
Ophtalmoscopie
Dans cette méthode d'examen des yeux, le praticien projette une lumière vive à travers la pupille dilatée et un ophtalmoscope fournit des images agrandies de la rétine. L'ophtalmoscopie est un outil de diagnostic important pour la DMLA car elle permet au praticien de voir les anomalies rétiniennes telles que l'atrophie, les drusens, les modifications pigmentaires et la néovascularisation choroïdienne (NVC).5,6 Il existe trois formes d'ophtalmoscopie.
Ophtalmoscopie directe
Dans l'ophtalmoscopie directe, le praticien fait passer une lumière vive à travers la pupille à l'aide d'un ophtalmoscope portatif.
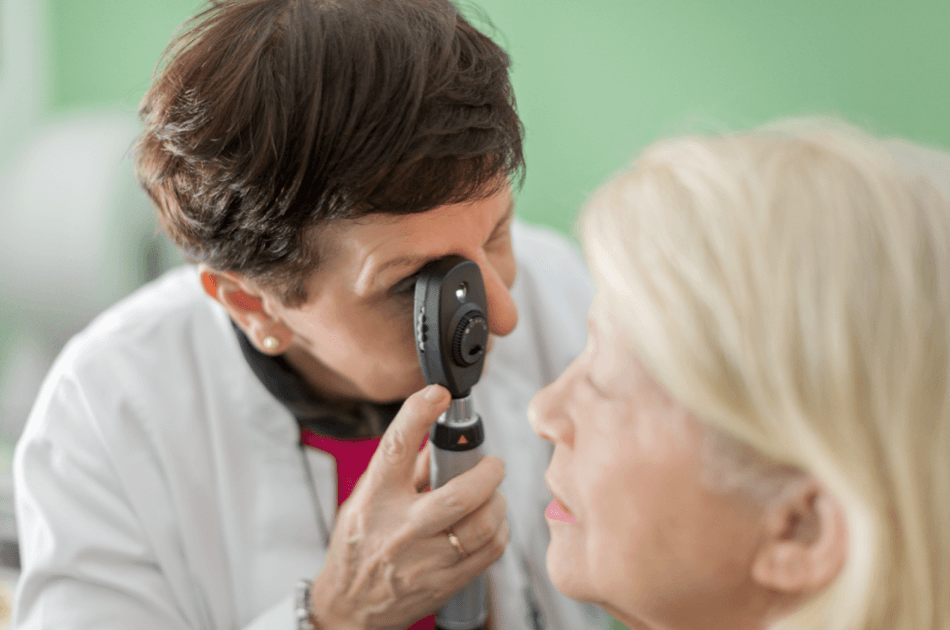
Ophtalmoscopie indirecte
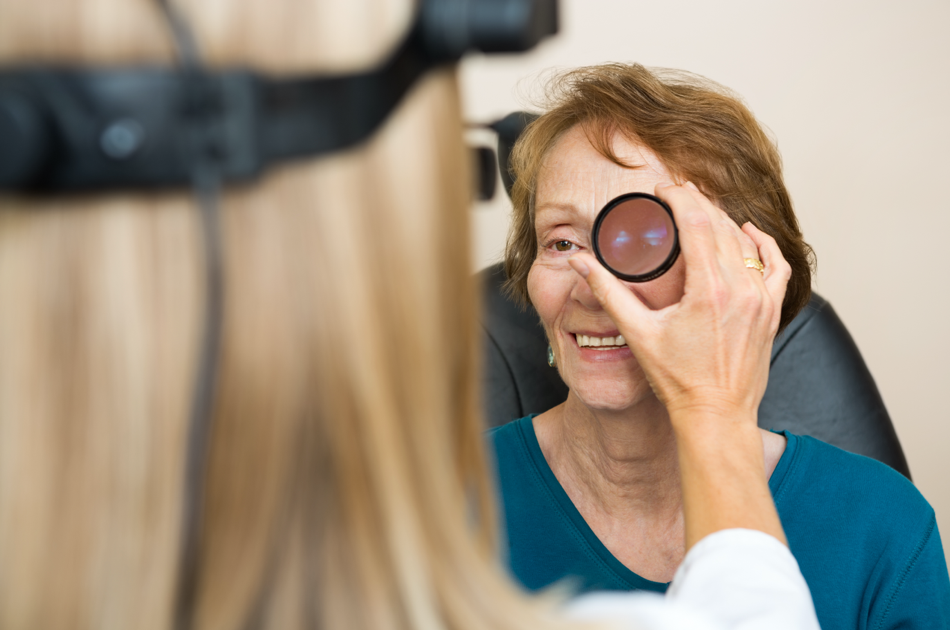
L'ophtalmoscopie indirecte est le type d'ophtalmoscopie le plus courant.5 Ici, le praticien envoie une lumière vive à travers la pupille à partir d'un ophtalmoscope monté sur la tête et utilise une lentille portative.5
Ophtalmoscopie à la lampe à fente
This type of examination is commonly used to Ce type d'examen, couramment utilisé pour diagnostiquer la DMLA, est réalisé avec un microscope ophtalmique à lampe à fente.5 Le menton du patient repose sur un dispositif à lampe à fente, la lumière est envoyée à travers une fente étroite dans l'œil du patient et le praticien examine le fond de l'œil à l'aide d'une loupe.5

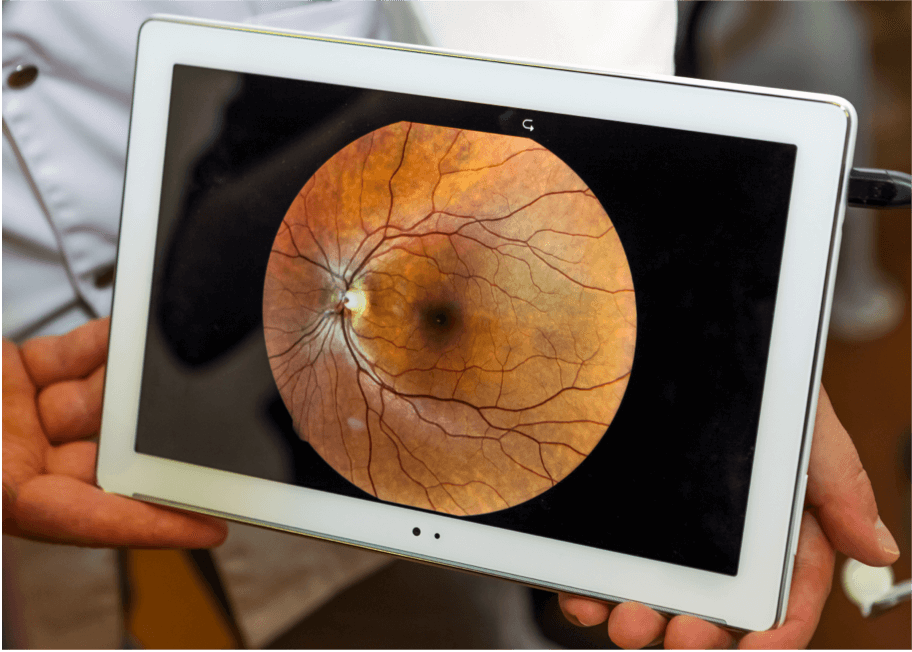
Photographie du fond de l'œil
La photographie du fond d'œil est réalisée à l'aide d'un microscope de faible puissance pour prendre des images en couleur de la rétine.7 Elle est couramment utilisée dans le diagnostic de la DMLA, car elle permet de mettre en évidence des anomalies rétiniennes telles que les drusens, les anomalies pigmentaires, l'atrophie, les saignements et l'accumulation de liquide.7 Les images prises au fil du temps peuvent être comparées pour suivre l'évolution de la maladie.
Modalités d'imagerie et manifestations
Il existe un certain nombre de techniques d'imagerie qui permettent une visualisation plus détaillée de la rétine chez les personnes atteintes de DMLA. Ces techniques permettent aux praticiens d'évaluer le stade et la gravité de la maladie au moment du diagnostic, ainsi que de suivre l'évolution de la maladie dans le temps.
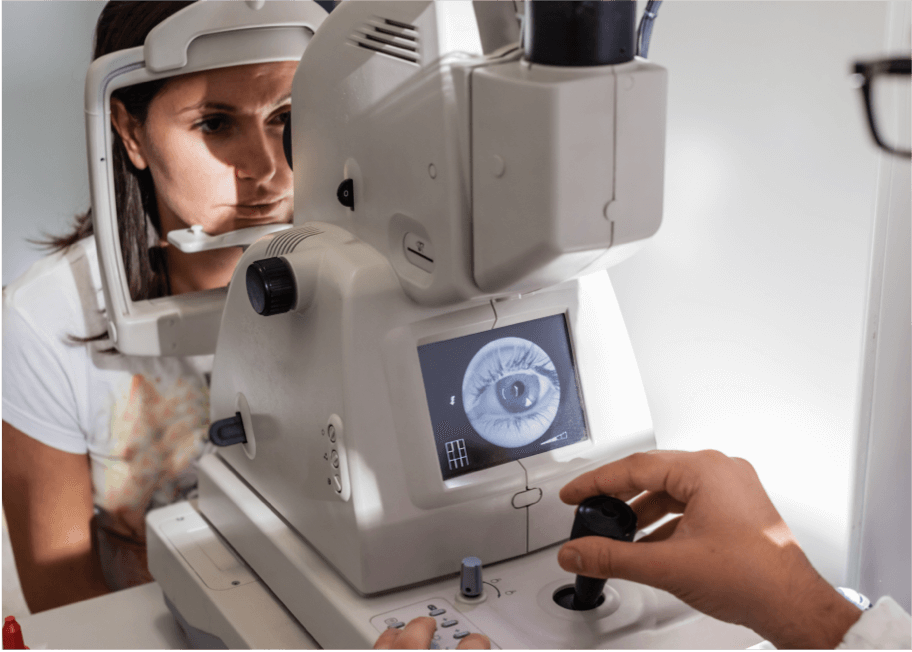
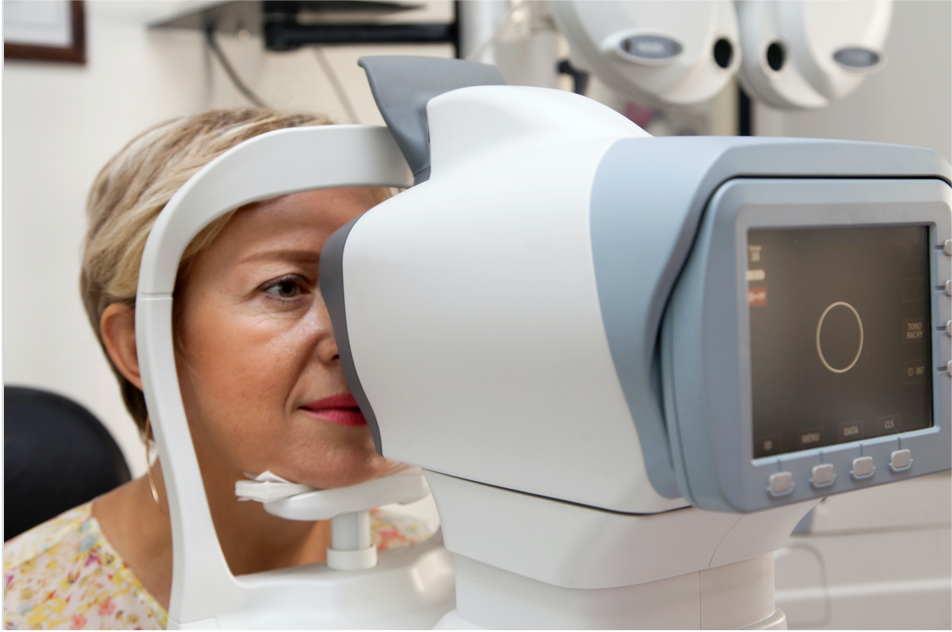
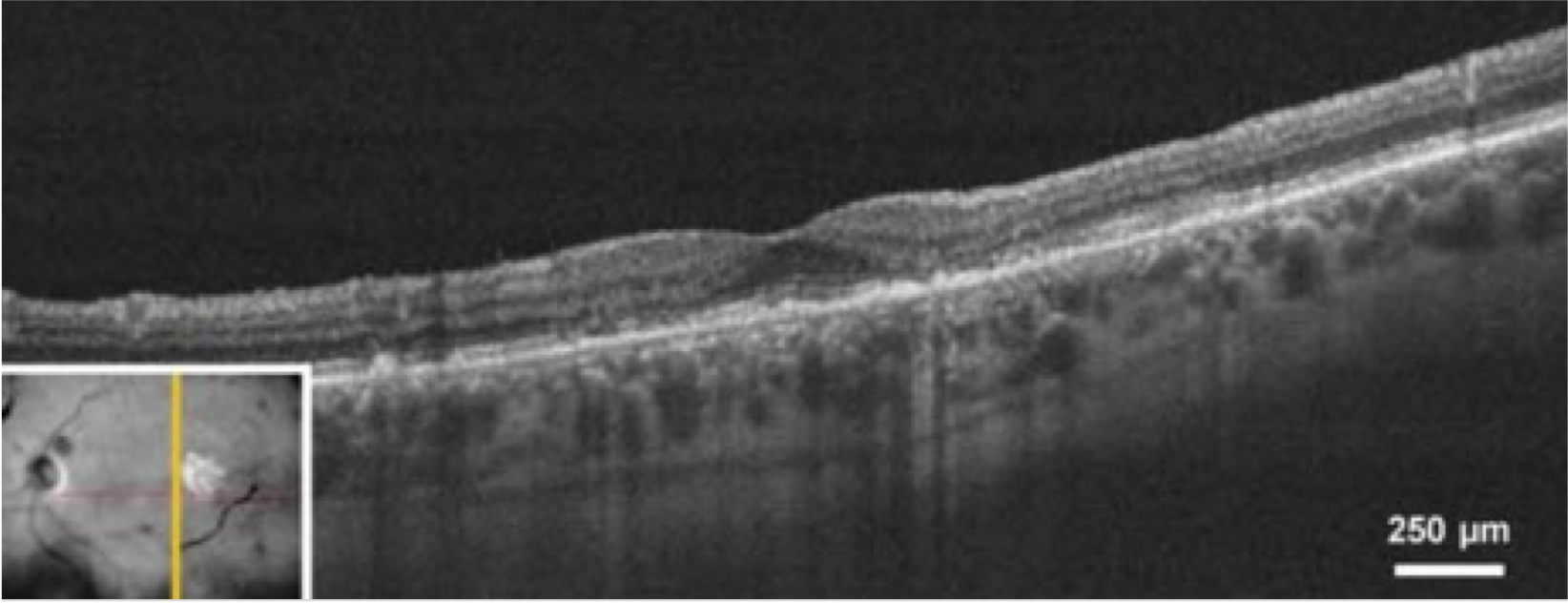
Tomographie par cohérence optique (OCT)
L'OCT est une technique d'imagerie importante pour le diagnostic et le suivi de la DMLA. Il prend des photos en coupe de la rétine et fournit une évaluation détaillée de la santé de la rétine. L'OCT peut mesurer l'épaisseur de la rétine, identifier les drusens et la néovascularisation choroïdienne (NVC), qui sont des caractéristiques typiques de la DMLA.8,9
Angiographie à la fluorescéine du fond de l'œil (FFA)
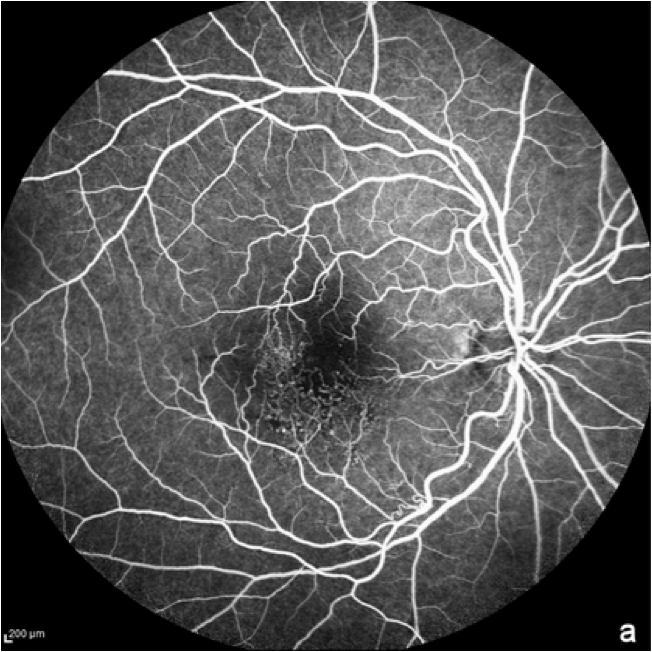
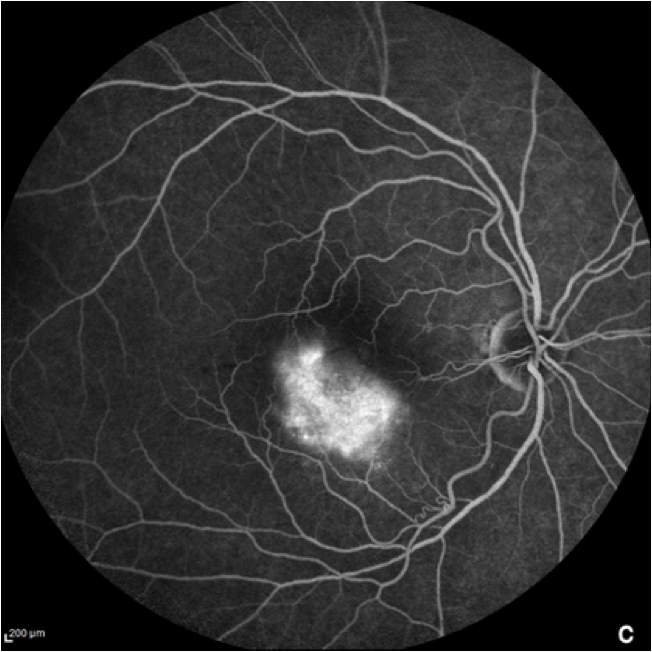
Dans l'angiographie à la fluorescéine, un colorant fluorescent est injecté par voie intraveineuse pour obtenir une image des vaisseaux sanguins de la rétine.11 L'angiographie à la fluorescéine est généralement utilisée pour exclure un diagnostic de DMLA humide. Il peut également être utilisé en cas de DMLA sèche avancée ou d'atrophie géographique, car les régions atrophiées présentent une fluorescence accrue en raison de la mort de l'épiphyllum pigmentaire rétinien (EPR).8
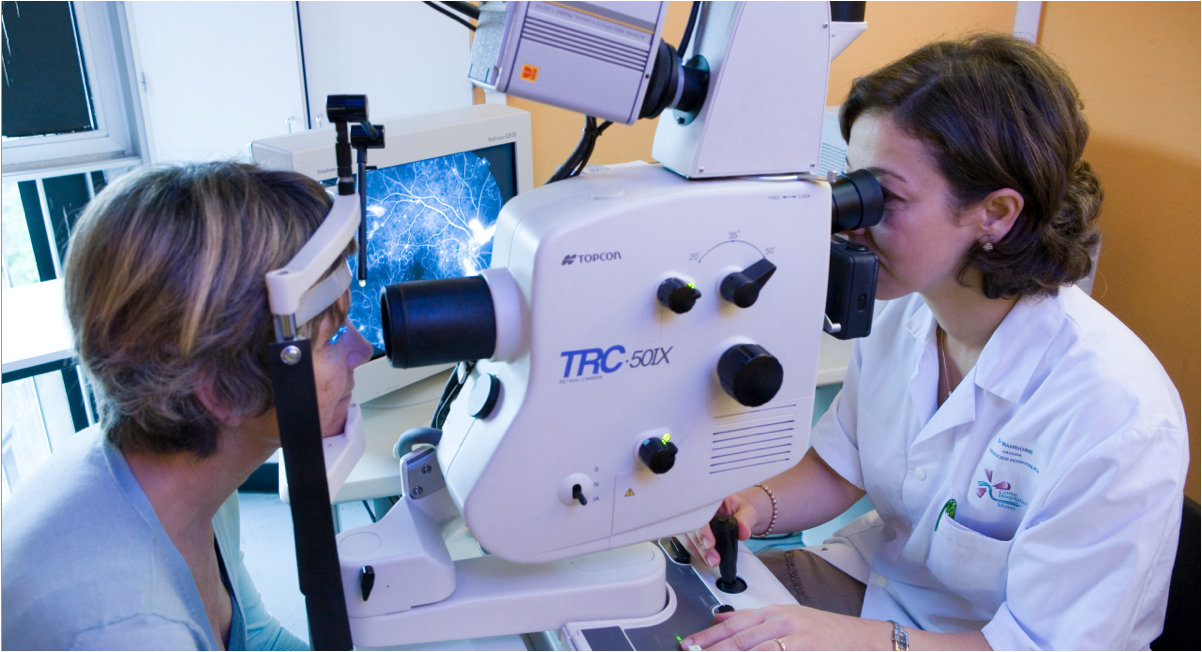
Les images FFA montrent les détails de la vascularisation de la rétine, ainsi que l'élimination du colorant dans les parties normales de la rétine et la persistance de la fluorescence dans les zones présentant des anomalies rétiniennes.12
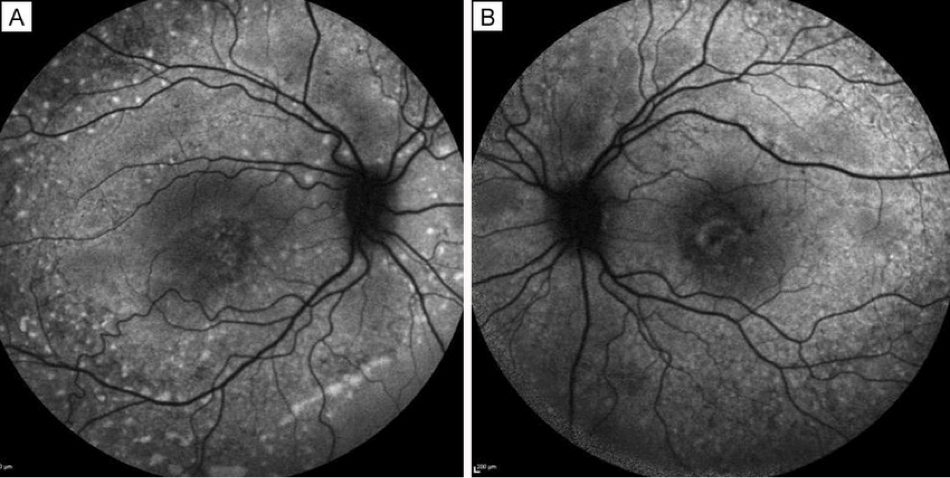
Autofluorescence du fond d'œil
L'autofluorescence du fond d'œil est une technique d'imagerie importante pour le diagnostic et le suivi de la DMLA, en particulier la DMLA sèche avancée ou DMLA atrophique.11 Une lumière spécifique (normalement bleue) est utilisée pour produire l'autofluorescence d'une molécule appelée lipofuscine, qui est généralement répartie uniformément dans la rétine.8 Les régions rétiniennes malsaines peuvent apparaître plus sombres pour les zones atrophiques, ou plus claires pour les drusens, qui sont tous deux des signes de DMLA.8,13 Le schéma de fluorescence peut indiquer le taux de progression potentiel de la DMLA chez un patient.14
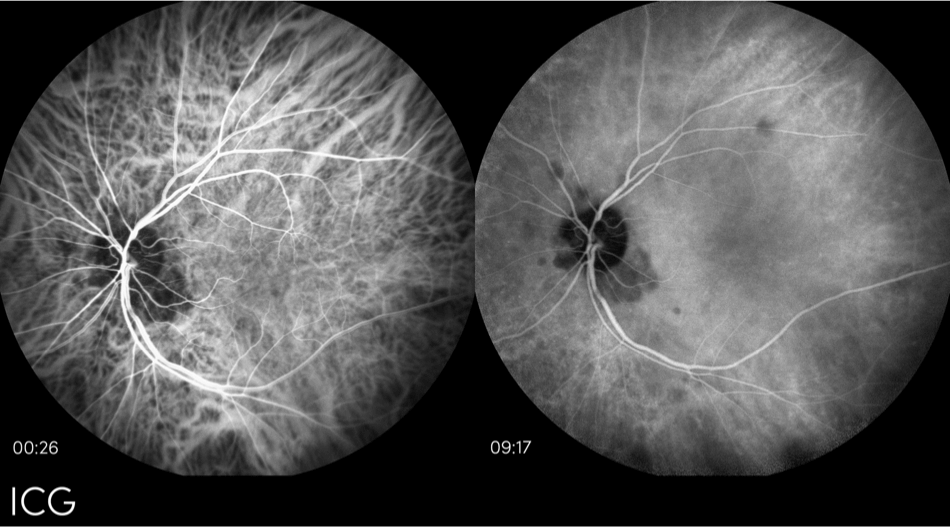
Angiographie au vert d'indocyanine (ICG)
ICG is is an imaging technique used to exclude wet AMD and also assess atrophic lesions in advanced dry L'ICG est une technique d'imagerie utilisée pour exclure la DMLA humide et également évaluer les lésions atrophiques dans la DMLA sèche avancée pour exciter la fluorescence, bien que l'angiographie ICG utilise un colorant injectable dans le flux sanguin et permette une meilleure résolution de l'image.13
Tests fonctionnels supplémentaires
En plus des tests de vision décrits ci-dessus, d'autres examens fonctionnels peuvent être utilisés pour surveiller la fonction visuelle des personnes atteintes de DMLA et évaluer l'impact sur leur vie quotidienne.
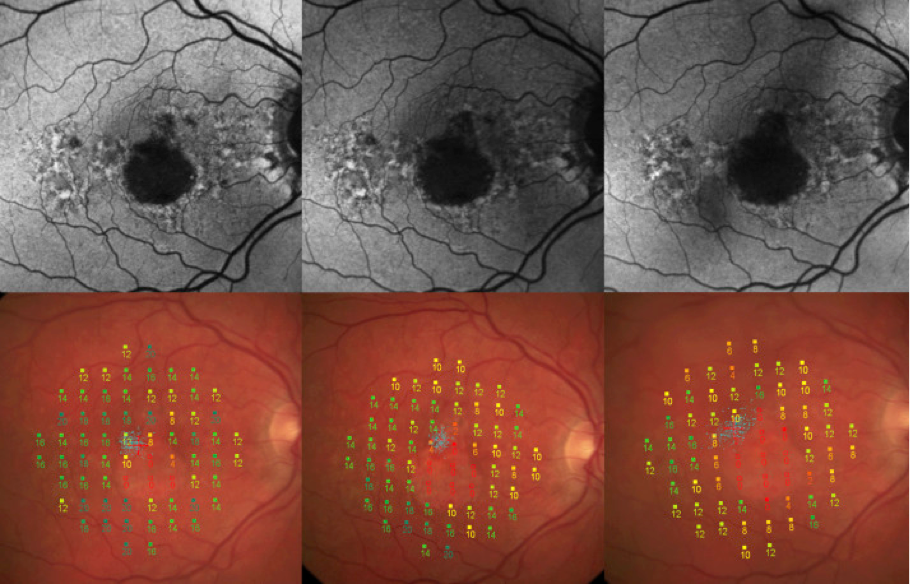
Microperimétrie
La microperimétrie évalue la capacité de l'œil à percevoir les stimuli lumineux dans différentes parties de la rétine. Il s'agit d'un appareil d'imagerie rétinienne avec un test de champ visuel permettant de cartographier spatialement la fonction des photorécepteurs. Les photorécepteurs sont les cellules sensibles à la lumière de la rétine. En microperimétrie, la rétine est exposée à de petites taches de lumière de différentes intensités. En appuyant sur un bouton, le patient reconnaît la perception du stimulus lumineux.15 Les éventuelles pertes de champ visuel sont alors identifiées sur la rétine de la personne.15
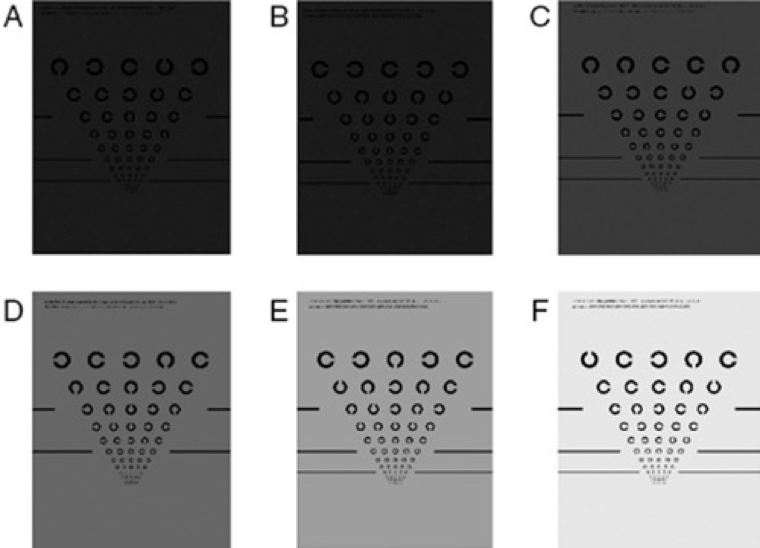
Acuité visuelle à faible luminosité (LLVA)
L'acuité visuelle des personnes atteintes de DMLA est généralement réduite dans des conditions de faible luminosité.8 Comme son nom l'indique, l'acuité visuelle à faible luminosité mesure la fonction visuelle dans des conditions de faible éclairage. Comme pour l'acuité visuelle mieux corrigée (BCVA), les patients regardent un tableau oculaire, mais avec la LLVA, cela se fait à travers des filtres qui réduisent les niveaux de lumière.16 La différence entre l'acuité visuelle mesurée en lumière vive (BCVA) et l'acuité visuelle mesurée en lumière faible est calculée et identifiée comme le déficit de luminescence faible (LLD).17 Le LLD d'une personne peut être corrélé aux lésions de la DMLA.17 Les personnes aux premiers stades de la DMLA ont tendance à obtenir de moins bons résultats à l'examen LLVA qu'à l'examen BCVA.17
Le tableau d'acuité MNRead ou le tableau de lecture basse vision du Minnesota
Dans la vie quotidienne, la diversité des tailles de texte peut être un véritable défi pour les personnes atteintes de DMLA, car elles éprouvent généralement des difficultés à maintenir une bonne vitesse de lecture. Le tableau d'acuité MNRead mesure la vitesse de lecture d'un individu en fonction de la taille des caractères. Une personne lit à haute voix des phrases dans des tailles de police décroissantes à partir d'un tableau. Le moment où la vitesse de lecture diminue avec une taille de police plus petite correspond à sa capacité visuelle.

Examen de la sensibilité aux contrastes
L'examen de la sensibilité aux contrastes utilise le tableau de sensibilité aux contrastes de Pelli-Robson. Ce tableau utilise des lettres de la même taille en progressant d'un contraste élevé à un contraste faible.18 Plus il est difficile pour une personne de distinguer les lettres, plus sa sensibilité au contraste est faible. Dans le cas de la DMLA, les examens de sensibilité au contraste permettent de détecter des anomalies visuelles qui pourraient ne pas être saisies lors d'un examen de l'acuité visuelle.19

L'indice d'indépendance fonctionnelle Reading (FRI1)
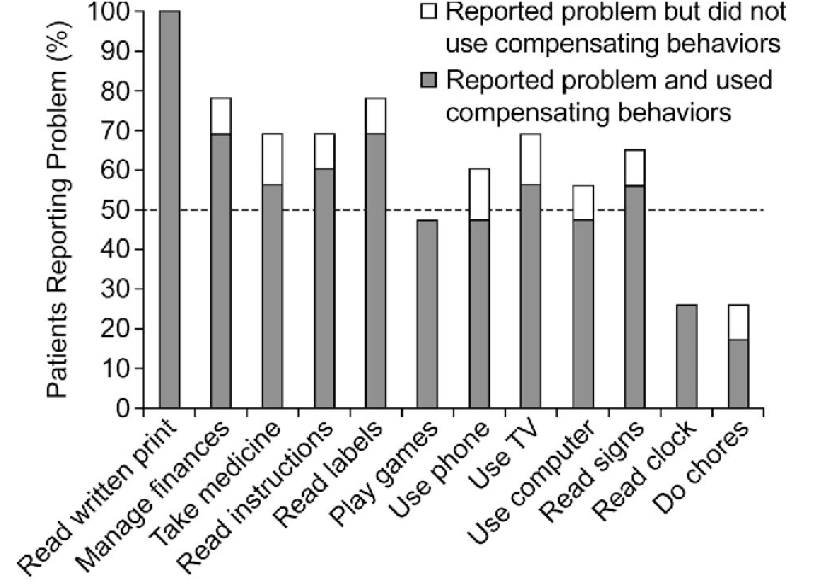
Le Functional Reading Independence (FRI) Index est une mesure rapportée par le patient qui évalue la capacité d'une personne atteinte d'AG à lire dans le cadre de diverses activités liées à la lecture.20
Les paramètres de la FRI comprennent la lecture d'étiquettes sur des flacons de médicaments ou des étiquettes alimentaires, la lecture pour mener et rédiger des examens, et lire des mots sur une télévision ou un ordinateur.20 Cette mesure est particulièrement importante pour les personnes atteintes de DMLA sèche avancée ou de DMLA atrophique qui peuvent souvent présenter des déficits visuels qui ne sont pas pris en compte par la BCVA.
Ressources et liens utiles
Références:
- Have AMD? Save Your Sight with an Amsler Grid. Accessed Nov. 15, 2021.
https://www.aao.org/eye-health/tips-prevention/facts-about-amsler-grid-daily-vision-test - Apellis GA Dossier Section 8.3 2.
- Lakshminarayanan, V. Visual acuity. in Handbook of Visual Display Technology vol. 1 93–99 (Springer Berlin Heidelberg, 2012).
- Mitchell P, Liew G, Gopinath B, Wong TY. Age-related macular degeneration. The Lancet. 392(10153):1147-59.
- American Academy of Ophthalmology. What is the difference between direct and indirect ophthalmoscopy? https://www.aao.org/eye-health/ask-ophthalmologist-q/what-is-difference-between-direct-indirect-ophthal. Published September 12, 2016. Accessed August 12, 2020.
- American Academy of Ophthalmology. What is a Slit Lamp? https://www.aao.org/eye-health/treatments/what-is-slit-lamp Published April 23, 2018. Accessed August 12, 2020.
- Townsend WD. Scleral depression. Optom Clin. 1992; 2(3);127-44 (1992).
- Fleckenstein M, Mitchell P, Freund KB. The progression of geographic atrophy secondary to age-related macular degeneration. Ophthalmology. 2018;125:369-90.
- Garcia-Layana A, Ciuffo G, Zarranz-Ventura J, Alvarez-Vidal A. Optical coherence tomography in age-related macular degeneration. www.amdbook.org. https://amdbook.org/content/optical-coherence-tomography-age-related-macular-degeneration. Updated July 2017. Accessed August 12, 2020.]
- Boyer DS, Schmidt-Erfurth U, van Lookeren Campagne M, Henry EC, Brittain C. THE PATHOPHYSIOLOGY OF GEOGRAPHIC ATROPHY SECONDARY TO AGE-RELATED MACULAR DEGENERATION AND THE COMPLEMENT PATHWAY AS A THERAPEUTIC TARGET. Retina. 2017 May;37(5):819-835. doi: 10.1097/IAE.0000000000001392. PMID: 27902638; PMCID: PMC5424580.
- Flaxel CJ, Adelman RA, Bailey ST, et al. AMD preferred practice pattern®. Ophthalmology. 2019.
- Bennett TJ. Interpretation. Ophthalmic Photographers’ Society website. 2019. Accessed September 9, 2020. https://www.opsweb.org/page/FAinterpretation
- Holz FG, Sadda SR, Staurenghi G, et al. Imaging protocols in clinical studies in advanced AMD: recommendations from classification of atrophy consensus meetings. Ophthalmology. 2017;124(4):464-78.
- Holz FG, Bindewald-Wittich A, Fleckenstein M, et al. Progression of geographic atrophy and impact of fundus autofluorescence patterns in AMD. Am J Ophthalmol. 2007;143(3):463-72.
- Csaky, K. G. et al. Microperimetry for geographic atrophy secondary to AMD. Surv. Ophthalmol. 2019;64, 353-64. 2. Apellis doc. Modules Conent_Modules 6 Conent d3.
- Sadda SR, Chakravarthy U, Birch DG, Staurenghi G, Henry EC, Brittain C. Clinical endpoints for the study of geographic atrophy secondary to AMD. Retina. 2016;36(10):1806-22.
- Wu Z, Ayton LN, Luu CD, Guymer RH. Longitudinal changes in microperimetry and low luminance visual acuity in AMD. JAMA Ophthalmol. 2015;133:442–48.
- Monés J, Rubin GS. Contrast sensitivity as an outcome measure in patients with subfoveal choroidal neovascularisation due to AMD. Eye (Lond). 2005;19(11):1142-50.
- Sunness JS, Rubin GS, Broman A, Applegate CA, Bressler NM, Hawkins BS. Low luminance visual dysfunction as a predictor of subsequent visual acuity loss from geographic atrophy in AMD. Ophthalmology. 2008 Sep;115(9):1480-8, 1488.e1-2.
- Kimel M, Leidy NK, Tschosik E, et al. Functional Reading Independence (FRI) Index: a new patient-reported outcome measure for patients with geographic atrophy. Invest Ophthalmol Vis Sci. 2016;57:6298-304.
EU-GA-2100012